(En Poblete, R., Patología Arterial y Venosa, Sociedad de Cirujanos de Chile, A. Yuri, Ed., Santiago, Chile, 1994: 479-503)
Peet en 1956 propone utilizar el término "Síndrome del opérculo torácico" (1) que considera adecuado para referirse a una serie de cuadros que, en una u otra forma, pueden ser capaces de comprimir el paquete neurovascular de la extremidad superior a nivel del estrecho desfiladero costo clavicular.
El término deriva de latín y se refiere al "orificio superior o tapa" del tórax; aunque lejos de ser él mejor, ha sido aceptado ampliamente ya que permite incluir en el múltiples entidades conocidas previamente bajo denominaciones muy diversas tales como síndromes de costilla cervical, síndromes del escaleno anterior, síndromes costoclaviculares, síndromes de primera costilla, síndromes de hiperabducción, síndromes hombro-brazo, síndromes de compresión cérvico-braquial, trombosis venosa de esfuerzo o síndromes de Pagett-Schroetter, síndromes de Addson, parálisis de Rucksack o síndromes de clavícula fracturada (2).
INCIDENCIA Y DISTRIBUCIÓN
Se trata de una condición cuyo significado e incidencia real resultan difíciles de precisar en la población general por su tendencia a manifestarse muchas veces sólo a través de una escasa sintomatología leve, pero que cuando se hace evidente especialmente por la aparición de alguna de sus potenciales complicaciones vasculares dista mucho de constituir una entidad benigna, pudiendo atribuírsele el 4.2 % de todas las isquemias de las extremidades superiores y buena parte de las trombosis venosas primarias de éstas (3, 4, 5).
La enfermedad se presenta principalmente en mujeres (relación de 2:1) y preferentemente en su opérculo derecho pero pueden ser también bilaterales, aunque en estos casos su magnitud rara vez resulte simétrica; se presentan especialmente entre los 13 y 55 años de edad, con una media de 36 años, exhibiendo en ocasiones una clara tendencia familiar.
ETIOPATOGENIA
La particular disposición del paquete neurovascular de la extremidad superior hace que, en el curso de su trayecto hacia la axila éste atraviese la región del opérculo torácico donde transcurre íntimamente relacionado con otras estructuras, principalmente óseas y de disposición casi horizontal como son la clavícula y el músculo subclavio por arriba, y el borde superior de la primera costilla por abajo; en su camino, se relaciona además con estructuras musculares de disposición vertical, como el escaleno medio que forma el límite posterior de éste espacio, y el escaleno anterior, que al insertarse en el tubérculo de Lisfranc del arco anterior de la primera costilla divide éste espacio en dos, dejando la vena subclavia por delante y la arteria y las ramas del plexo braquial por detrás de él (Figuras 1 y 2).
 Figura 1. Aspectos anatómicos de la región del opérculo torácico.
Figura 1. Aspectos anatómicos de la región del opérculo torácico. Figura 2. Relación de las estructuras del paquete neurovascular de la extremidad entre sí, y con las estructuras vecinas
Figura 2. Relación de las estructuras del paquete neurovascular de la extremidad entre sí, y con las estructuras vecinasEsta disposición anatómica puede ser distorsionada por la frecuente ocurrencia de ciertas variantes anatómicas en la región.
- La primera que fue descrita cronológicamente, es la presencia de una costilla cervical, que con cierta frecuencia aunque no siempre puede alterar la anatomía, tanto en forma mecánica como a través de las bandas fibrosas anómalas que la acompañan y que, desde su vértice se extienden hacia delante, describiendo una curva por debajo del plexo braquial al que pueden eventualmente comprimir, hasta insertarse en el tubérculo del escaleno del arco anterior de la primera costilla (Figuras 3 y 4).
 Figura 3 a-c: Costilla cervicales. a) Aspecto externo de una costilla cervical izquierda. b) Radiografía mostrando una costilla cervical derecha. c) Planigrafía mostrando una costilla cervical izquierda.
Figura 3 a-c: Costilla cervicales. a) Aspecto externo de una costilla cervical izquierda. b) Radiografía mostrando una costilla cervical derecha. c) Planigrafía mostrando una costilla cervical izquierda.


Figura 4. Esquema de la compresión neural más frecuente de encontrar en presencia de una costilla cervical.
- Idéntico fenómeno puede ocurrir en individuos con sus apófisis transversas de la séptima vértebra extremadamente largas, cuando bandas fibrosas anómalas unirán el extremo de dicha apófisis con el tubérculo del escaleno (Figura 5).
 Figura 5. Radiografía simple. Presencia de una apófisis transversa de C7 extremadamente larga a la izquerda.
Figura 5. Radiografía simple. Presencia de una apófisis transversa de C7 extremadamente larga a la izquerda.Al respecto Roos (6) ha descrito en detalle, el tipo y distribución de estas bandas anómalas eventualmente compresivas, que afirma haber encontrado tanto en el 98 % de 241 intervenciones quirúrgicas realizadas por él para corregir éste síndrome, como al revisar 58 autopsias de portadores de ésta enfermedad, las que divide en 7 grupos diferentes:
- Tipo I: se presenta bajo la forma de un ligamento anómalo extendido desde el vértice de una costilla cervical hacia el tubérculo del escaleno (8 % de los casos).
- Tipo II: se trata de un ligamento de características similares, pero extendido desde el vértice de una apófisis transversa larga de C7 hacia el tubérculo del escaleno (4 %).
- Tipo III: sería la anomalía más común, representada por una banda fibrosa que se extiende como la cuerda de un arco desde el cuello de la primera costilla por atrás hacia el tubérculo del escaleno por delante (61 %).
- Tipo IV: consiste en una unión muscular anómala entre el escaleno medio y el anterior, capaz de rechazar la arteria subclavia y el plexo braquial hacia arriba o abajo (5 %).
- Tipo V: está representado por la presencia de un escaleno "mínimo" anómalo, que se dirige desde la apófisis transversa de C6 o C7 hasta el tubérculo del escaleno, separando la vena subclavia del plexo (17 %).
- Tipo VI: es la presencia del mismo escaleno mínimo, que en éste caso se encuentra fijado por delante en la cúpula pleural (17 %).
- Tipo VII: es el más escaso y consiste en la presencia de una banda muscular nacida del escaleno anterior, que pasa por debajo de la vena desviándola de su trayecto (1 %).
Cualquier variación importante en la posición, relación o tamaño de las estructuras anatómicas normales antes mencionadas, o la presencia de algunas anomalías en la región del opérculo torácico como las sugeridas por Roos, podrán inducir una compresión del paquete neurovascular capaz, según la causa que lo produzca, su localización y el sentido en el cuál actúa, de comprometer en forma preferente a uno u otro de sus componentes.
Este hecho puede explicar la poca constancia u ocasional asimetría de algunas manifestaciones de la enfermedad, que no necesariamente se presentará clínicamente en todos los casos de compresión anatómicamente demostrable, sino sólo en algunas de ellas que suelen corresponder a las más severas; explica también porqué en forma bastante selectiva las compresiones originadas por estructuras óseas se manifestarán preferentemente a través de una complicación arterial, mientras que la mayoría de las complicaciones venosas y neurológicas ocurrirán cuando la causa resida en la presencia de una banda fibrosa muscular anómala.
Aparte de la eventual presencia de bandas fibromusculares anómalas congénitas como principales responsables del síndrome, cabe destacar otros agentes etiológicos entre los que destacan las fracturas de clavícula o de primera costilla con callos exuberantes o consolidación viciosa, la presencia de costillas cervicales, los tumores de la clavícula y primera costilla (7), las anomalías de posición o forma de la primera costilla (8), algunas malformaciones torácicas como pectus carinatum, pectum excavatum y algunas escoliosis, las hipertrofias primarias del escaleno anterior y rara vez del escaleno medio y las malas posiciones posturales.
SINTOMATOLOGÍA
Deberá ser claramente diferenciada en dos grupos según sí la enfermedad se encuentra o no complicada en el momento del diagnóstico, ya que la inmensa mayoría de los pacientes se encontrará habitualmente libre aún de complicaciones.
En ambas eventualidades los síntomas traducirán el compromiso no siempre homogéneo de los diversos componentes del paquete neurovascular; así, las raíces destinadas a formar los nervios del plexo braquial serán afectadas en la casi totalidad de los pacientes, la vena subclavia con una incidencia francamente menor y muy rara vez la arteria, sin que sea infrecuente encontrar la presencia simultánea de síntomas mixtos, atribuibles al compromiso de más de una estructura.
- En el paciente no complicado predominan los síntomas neurológicos que, dependiendo de la causa que origina la compresión, se pueden traducir por un compromiso principalmente bajo del plexo braquial cuando la compresión afecta principalmente las raíces C8 y T1 o alto, si comprometen las raíces C5, C6 y C7.
Estos se manifiestan especialmente por dolor y severas parestesias, y en forma secundaria por una disminución de las fuerzas que son referidas a la mano de la extremidad comprometida.
Sin embargo el dolor puede comenzar incluso en la cintura escapular, irradiándose al dorso, cuello y región pectoral y extenderse a lo largo del brazo y antebrazo hacia los dedos, donde afecta aquéllos del área cubital y menos frecuentemente los del área del mediano y el radial, comprometiendo a veces todos los dedos.
Es característico que el dolor o las parestesias de la mano aumenten en grados variables durante la noche haciéndose a veces intolerables, por estrechar el decúbito el espacio costoclavicular; igual ocurre cuando se realizan maniobras que exigen mantener la extremidad elevada durante períodos prolongados, lo que hace difíciles tareas tan sencillas como leer un diario, peinarse, pintar un techo u ordenar un closet.
Existen otros síntomas neurológicos no descritos previamente que se encuentran con frecuencia y sobre cuya etiología sólo cabe especular.
El primero es un dolor atípico en la región lateral del cuello y que asciende hasta el área parietal, cuyo carácter resulta difícil de describir pero que el paciente suele homologar a una cefalea vascular o jaqueca, de las que la diferencia por su duración y curso paralelo a las parestesias de la extremidad; el otro, es la incapacidad de mantener la vista fija en forma prolongada en un mismo objeto distante, sugiriendo una dificultad en la acomodación, fenómeno capaz de hacer poco atractivas actividades como leer o ver televisión.
La disminución de las fuerzas resulta especialmente notoria en la mano y es producida principalmente por la denervación cubital y radial, advirtiéndose dificultades progresivas en el control de los movimientos finos de los dedos y al cerrar con fuerza la mano. Conforme la enfermedad progresa, se asistirá a la aparición de una impotencia muscular extensa de la extremidad que es capaz de ascender hasta la cintura escapular, haciendo entonces muy difícil la elevación de la extremidad o su desplazamiento hacia el dorso.
- En el paciente no complicado cabe reconocer algunos síntomas atribuibles a compresión venosa a nivel de la subclavia, como una notoria dilatación de las venas superficiales de la extremidad, de grado variable pero que se acentúa con la elevación del miembro y cierto grado de edema de las manos, especialmente notorio al despertar y que puede erróneamente interpretarse como rigidez interfalángica matutina, induciendo a pensar en alguna enfermedad reumatológica.
- Los síntomas que traducen una compresión arterial en el paciente no complicado son principalmente los fenómenos de palidez y un enfriamiento posicional de la mano, especialmente evidente durante la elevación de la extremidad, y en algunos casos la presencia permanente de un verdadero síndrome de Raynaud, el que muchas veces forma parte integrante del cuadro habitual.
COMPLICACIONES
En el paciente complicado las cosas serán absolutamente diferentes, ya que a la sintomatología previa se le sumará aquélla que refleja la complicación sobre agregada (9, 10).
- La compresión neurológica puede llevar lentamente a una denervación progresiva de la extremidad y, en casos excepcionales conducir a una severa impotencia muscular, especialmente notoria en la mano y debida a la atrofia de los músculos interóseos y de la eminencia tenar e hipotecar (Figura 6).
 Figura 6 a y b: Dos casos de denervación grave. a) Individuo de 22 años, con SOT bilateral. Se aprecia la atrofia de los interóseos y de la eminencia hipotear. b) Hombre de 60 años con síntomas durante 30 años. Se advierte la marcada atrofia de los interóseos.
Figura 6 a y b: Dos casos de denervación grave. a) Individuo de 22 años, con SOT bilateral. Se aprecia la atrofia de los interóseos y de la eminencia hipotear. b) Hombre de 60 años con síntomas durante 30 años. Se advierte la marcada atrofia de los interóseos.
Si bien su ocurrencia no es muy frecuente en los casos en que se produce resulta severa por su lenta recuperación.
- La complicación venosa no es tan infrecuente, llegando a presentarse en el 5 % de todos los portadores del síndrome (11); se manifiesta por la aparición de una trombosis venosa primaria de la extremidad, que puede ser de tipo masivo e instalada en el eje subclavio axilar o como en otras oportunidades manifestarse en forma más circunscrita, afectando tanto a las venas superficiales como profundas de la extremidad.
- La complicación arterial aparece con una incidencia menor que la venosa y casi siempre ocurre cuando la compresión se debe a la presencia de una costilla cervical u otras anomalías óseas y puede manifestarse bajo dos modalidades diferentes:
- La más común y al mismo tiempo de menor gravedad es la aparición aislada, o en forma recurrente, de microembolías digitales producidas por la fragmentación de pequeños émbolos que se alojan en las arterias digitales, los que se originaron al aparecer una solución de continuidad en la íntima de la subclavia a consecuencias del traumatismo repetido del vaso por el agente compresivo (Figura 7).
 Figura 7 a y b. Embolias digitales. a) Embolia de tres dedos de la mano derecha por una variante de SOT por bandas fibromusculares anómalas extremadamente grave. La arteriografía mostró una embolia de arterias digitales. b) Vista de los dedos, un mes después de la operación.
Figura 7 a y b. Embolias digitales. a) Embolia de tres dedos de la mano derecha por una variante de SOT por bandas fibromusculares anómalas extremadamente grave. La arteriografía mostró una embolia de arterias digitales. b) Vista de los dedos, un mes después de la operación.
Clínicamente la microembolia se manifiesta por la aparición de coloración ruborosa o cianótica en la porción distal o incluso en toda la extensión de uno o más dedos, acompañada por un edema moderado y un mínimo grado de impotencia funcional, al tiempo que se mantienen tanto la temperatura como la motilidad gruesa de la mano; el cuadro suele regresar en forma espontánea en los días siguientes sin dejar secuelas apreciables.
- La segunda variante de complicación arterial es poco frecuente pero extremadamente severa y se manifiesta por la aparición de una isquemia grave o extensa de los dedos o de buena parte de la extremidad producto de una embolia masiva. Esta puede tener su origen en el endotelio de la subclavia aprisionada en forma reiterada, en una dilatación postestenótica e incluso en un aneurisma verdadero de la subclavia, hechos que puede ocurrir en casos de compresión particularmente severa y prolongada (Figura 8).
 Figura 8. Angiografía subclavia izquierda en un SOT grave complicado por embolia del antebrazo, y que previamente había presentado una trombosis venosa axilar. Se advierte claramente, al elevar la extremidad, la presencia de una estenosis con dilatación postestenótica.
Figura 8. Angiografía subclavia izquierda en un SOT grave complicado por embolia del antebrazo, y que previamente había presentado una trombosis venosa axilar. Se advierte claramente, al elevar la extremidad, la presencia de una estenosis con dilatación postestenótica.Probablemente la complicación arterial de mayor peligro vital es la embolia masiva de la extremidad derecha originada en la subclavia, sitio desde el cuál accesoriamente por extensión proximal del trombo y fragmentación del émbolo es capaz de embolizar simultáneamente la carótida común, apareciendo en forma simultánea una isquemia de la extremidad derecha junto con una hemiparesia o hemiplegia izquierda por el infarto hemisférico derecho; sólo recientemente ha sido comunicada ésta temible complicación, que hemos tenido oportunidad de demostrar hasta ahora en algunas ocasiones en pacientes jóvenes, carentes riesgo y con el resto de los vasos enteramente normales (Figura 9).
 Figura 9. Arteriografía de un paciente de 51 años, sin factores de riesgo y portador de un SOT derecho grave, luego de presentar una doble embolia simultánea del brazo y cerebral. Se advierte la irregularidad de la subclavia donde se inició la trombosis.
Figura 9. Arteriografía de un paciente de 51 años, sin factores de riesgo y portador de un SOT derecho grave, luego de presentar una doble embolia simultánea del brazo y cerebral. Se advierte la irregularidad de la subclavia donde se inició la trombosis.EXAMEN FÍSICO
- Ocasionalmente se podrá palpar en el cuello una costilla cervical o una apófisis transversa larga, pero los signos usuales en la enfermedad son más bien escasos.
- La coloración de los dedos y de la mano, la sequedad de la piel y la fragilidad de las uñas característicos del Raynaud suelen estar presentes así como algún grado de dilatación venosa y edema de la mano.
- En el examen físico el hecho cardinal que sugiere el diagnóstico de éste síndrome es la posibilidad de reproducir el dolor y las parestesias en la localización particular descrita por cada paciente mediante maniobras simples, como es la percusión del escaleno anterior o su compresión contra la columna vertebral.
- El test de hiperabducción forzada de las extremidades es el más específico para demostrar tanto la compresión neural como vascular; si resulta positivo rara vez es tolerado por más de tres minutos cuando la compresión neurovascular es severa, y podrá advertirse que al tiempo que se realiza aparecerán progresivamente los síntomas neurológicos del paciente, quién llegará prontamente a un agotamiento muscular. Además suele ser posible apreciar que, mientras se ejecuta, aparecen en forma bastante evidente tanto la palidez posicional de la mano como un aumento de la dilatación venosa de las extremidades.
-La maniobra de Adson, consistente en evaluar el pulso radial en cada lado, al tiempo que se solicita al enfermo que inspire y gire la cabeza hacia ese mismo lado o hacia el opuesto, suele permitir apreciar una reducción de la amplitud del pulso.
- El test costoclavicular, que consiste en adoptar la posición erguida con los hombros dirigidos hacia atrás simulando el uso de una mochila, también puede revelar a veces disminución del pulso en la extremidad comprometida.
En presencia de algunas complicaciones el diagnóstico resulta más fácil, por el hallazgo de atrofia muscular y severa reducción de las fuerzas de la mano, la presencia de una trombosis venosa, microembolías, ulceraciones o necrosis distales de la extremidad.
DIAGNÓSTICO
El diagnóstico suele ser fácil en la mayoría de los casos complicados, pero difícil en aquéllos que no lo están.
En éstos últimos resulta indispensable certificar la presencia de una compresión a nivel del opérculo torácico al tiempo que descartar cualquier otro cuadro capaz de simular ésta condición, lo que no siempre resulta fácil de obtener.
Pueden simular el síndrome algunas afecciones preexistentes como son las frecuentes espondilosis cervicales, hernias del núcleo pulposo o raquiestenosis, el síndrome del túnel carpiano (12), las miositis, bursitis, fibrositis, neuritis, tendinitis, el síndrome del manguito de los rotadores, algunas neurosis y el síndrome de Raynaud primario, aparte de enfermedades como la esclerosis múltiple, tumores medulares y el tumor de Pancoast, entre otras.
Podrán contribuir al diagnóstico los siguientes exámenes complementarios:
- Radiografías de tórax y columna cervical: la primera permite apreciar eventuales anomalías de la clavícula o de la primera costilla y, al igual que la segunda, ayuda a descartar otra patología.
Es básicamente una forma de evaluar el componente anatómico de la enfermedad. Suele resultar característica de la enfermedad la demostración de que las primeras costillas se encuentran en una posición más vertical que lo usual, y muchas veces en los casos de larga data ensanchadas en su extremo anterior a la manera de una cimitarra (Figura 10).
 Figura 10 a y b: a) Aspecto radiológico característico del síndrome del opérculo torácico. Las primeras costillas son más anchas que lo normal en su extremo anterior, y descienden más verticalmente que lo usual. Además, las clavículas son más horizontales que lo acostumbrado. B) Otra placa simple de tórax demostrando el mismo hecho.
Figura 10 a y b: a) Aspecto radiológico característico del síndrome del opérculo torácico. Las primeras costillas son más anchas que lo normal en su extremo anterior, y descienden más verticalmente que lo usual. Además, las clavículas son más horizontales que lo acostumbrado. B) Otra placa simple de tórax demostrando el mismo hecho.
- TAC: no resulta indispensable, aunque su ocasional ejecución ayuda a descartar patología de otra naturaleza y puede permitir ocasionalmente observar algunas anomalías óseas o musculares de la región.
- Estudio no invasivo dinámico de las extremidades superiores, con fotopletismografía:
Resulta excelente para evaluar el componente arterial de la enfermedad y objetivar la severidad de la reducción de flujo arterial durante la ejecución de los test de hiperabducción a 90 y 180°, costoclavicular y de Adson. La presencia de una compresión arterial en reposo, o una que aparezca durante la movilización dinámica de la extremidad se traducirá en una reducción variable del flujo periférico, el que puede llegar a desaparecer incluso completamente en los casos severos (Figura 11).
 Figura 11. Fotopletismografía dinámica preoperatorio de un SOT bilateral.
Figura 11. Fotopletismografía dinámica preoperatorio de un SOT bilateral.En nuestra experiencia el test más sensible para la evaluación arterial ha resultado ser el de hiperabducción, ya que es capaz de alterarse incluso en presencia de compresiones de poca magnitud; al mismo tiempo, hemos aprendido que una compresión neurovascular será muy severa en cada oportunidad en que los tres test se vean alterados.
- Flebografía ascendente dinámica de la extremidad: tratándose de un método poco invasivo y sencillo de ejecutar resulta de enorme valor para evaluar el componente venoso de la enfermedad cuando la compresión venosa sea el hecho mas relevante y el estudio no invasivo no sea categórico.
Se realiza inyectando medio de contraste a través de una vena periférica superficial en forma de bolos mientras la extremidad se dispone en posición de reposo, en 90 grados y en hiperabducción; el contraste iónico debe normalmente difundir con rapidez hacia la vena axilar, subclavia y la cava superior revelando el lúmen de éstas venas cuyo diámetro normalmente aumenta paulatinamente sin que se haga evidente ninguna deformación de sus contornos, cualquiera sea la posición en que se estudie el miembro.
El examen podrá demostrar algunas válvulas venosas de caracteres normales y en contados casos la presencia de trombos en las venas superficiales o profundas de la extremidad, pero esto no constituye el objetivo básico del examen que es la verificación del sitio exacto en que se produce la compresión venosa y su magnitud.
La demostración de un avance lento del medio de contraste hacia la cava, o su reflujo hacia las venas profundas distales del miembro son indicadores indirectos de la presencia de una compresión objetiva de la subclavia capaz de dificultar el drenaje venoso de la extremidad, cualquiera sea la posición en que se presente, aunque resulta especialmente notable durante la elevación de la extremidad.
Cuando la compresión es severa se advertirá una deformación anterior, posterior, superior o inferior de la subclavia, provocada por la compresión extrínseca capaz de actuar en uno u otro sentido y cuyo grado puede ser muy variable, oscilando entre una irregularidad mínima hasta una estrechez severa en reloj de arena y que, de acuerdo al sentido de la compresión permite a veces deducir la etiología de la enfermedad en ese caso en particular (Figura 12).
 Figura 12 a y b: Flebografía dinámica de la extremidad superior izquierda. a) Extremidad en aducción. Se advierte el reflujo del contraste y ya se aprecia una estrechez. b) Con la extremidad elevada la compresión se hace más nítida, aunque el reflujo ahora ha desaparecido.
Figura 12 a y b: Flebografía dinámica de la extremidad superior izquierda. a) Extremidad en aducción. Se advierte el reflujo del contraste y ya se aprecia una estrechez. b) Con la extremidad elevada la compresión se hace más nítida, aunque el reflujo ahora ha desaparecido.
- Eco doppler: por su capacidad para medir la velocidad del flujo resulta un método novedoso para detectar tanto compresión arterial como venosa susceptible de aparecer durante la movilización dinámica de la extremidad, aunque sea incapaz de ofrecer una información anatómica o etiológica más precisa del fenómeno, e incapaz de detectar las compresiones predominantemente neurales que son las que prácticamente siempre caracterizan éste síndrome.
- Arteriografía dinámica de la extremidad: tratándose de un método invasivo deberá reservarse solamente para aquéllos casos severos con clara indicación quirúrgica, especialmente si son de larga data y cuando la auscultación supraclavicular haga sospechar la presencia de un aneurisma post estenótico en la subclavia. Debe realizarse siempre también en aquéllos casos que hayan tenido alguna complicación arterial previa (Figuras 13 y 14).
 Figura 13 a y b: Angiografía dinámica en un SOT grave desde el punto de vista neurológico. a) Con el brazo abajo. b) Al elevar la extremidad, la estenosis subclavia se hace muy evidente.
Figura 13 a y b: Angiografía dinámica en un SOT grave desde el punto de vista neurológico. a) Con el brazo abajo. b) Al elevar la extremidad, la estenosis subclavia se hace muy evidente.
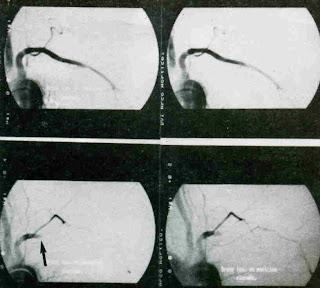 Figura 14 a y b: Arteriografías dinámicas de dos pacientes diferentes con un SOT izquierdo. a) La compresión arterial, casi ausente en reposo, interrumpe totalmente el flujo al elevar la extremidad. b) En este caso, con la elevación de la extremidad aparece una imagen en reloj de arena en la subclavia.
Figura 14 a y b: Arteriografías dinámicas de dos pacientes diferentes con un SOT izquierdo. a) La compresión arterial, casi ausente en reposo, interrumpe totalmente el flujo al elevar la extremidad. b) En este caso, con la elevación de la extremidad aparece una imagen en reloj de arena en la subclavia.
- Electromiografía: se utiliza rara vez con la intención de confirmar el diagnóstico por su incapacidad para evaluar en forma precisa el componente neurológico de la enfermedad, aún cuando puede resultar útil en algunos casos para descartar otra patología neurológica periférica o central. La velocidad de conducción del nervio cubital es capaz de sugerir compresión sólo cuando se encuentra reducida por debajo de los 70 m/seg., sin que pueda ser considerada diagnóstica por la gran amplitud del rango que se ha constatado en los portadores de la enfermedad debidamente documentados (13, 14), así como también la velocidad de conducción del mediano es demasiado variable para resultar útil.
Igual problema plantea el estudio de los potenciales evocados sómato sensitivos en éstos pacientes, los que nos han resultado de poca utilidad para asegurar compromiso neurológico debido a ésta causa. Es de interés destacar que no es raro encontrar que pacientes con sus tiempos de conducción alterados y que han sido operados obteniendo un completo alivio sintomático y la desaparición objetiva de la compresión, pueden persistir durante largo tiempo con su electromiografía alterada sin llegar a obtener una normalización de la conducción eléctrica hasta muchos años después, lo cuál hace que el examen tampoco sea útil para el seguimiento alejado del paciente.
- Cintigrafía isotópica: si bien es capaz de mostrar un retardo en el avance del medio de contraste hacia el tórax, resulta ser demasiado inespecífico como para su empleo rutinario en el estudio de ésta enfermedad.
TRATAMIENTO
TRATAMIENTO MÉDICO
La inmensa mayoría de los portadores del síndrome que no hayan presentado complicaciones neurológicas, venosas o arteriales, serán beneficiados por un tratamiento kinésico dirigido a obtener una ampliación del espacio costoclavicular a expensas de la elongación de las estructuras musculo-aponeuróticas y bandas fibromusculares causantes del estrechamiento y la compresión.
Este debe ser realizado inicialmente por kinesiólogos conocedores del tema, y apoyado con ultrasonido cada vez que haya espasmo muscular, única forma de asegurar su efectividad; luego ése tratamiento debe ser seguido por el paciente durante no menos de cuatro meses, y en algunos casos en forma indefinida.
- El tratamiento médico es particularmente efectivo en pacientes con síntomas neurológicos y velocidad de conducción normal o con síntomas venosos o arteriales de poca magnitud, quiénes podrán mejorar completamente y en forma definitiva en cerca del 90 % de los casos, siempre que no abandonen la terapia.
- Las otras medidas útiles se relacionan con el uso de relajantes musculares intentando aliviar el espasmo, evitar la hiperabducción de la extremidad cada vez que sea posible, y el empleo de un cojín cervical para dormir que siendo de poca altura, de forma trapezoidal y gracias a la diversa densidad de la espuma que contienen, permite un alivio considerable de las parestesias y el dolor al mantener la musculatura cervical elongada durante el sueño.
TRATAMIENTO KINÉSICO
La metódica propuesta por Redford al respecto (15) nos ha permitido obtener resultados muy gratificantes, y como su práctica no demora más de 15 minutos puede ser realizada una o dos veces por día. Consta de tres grupos de ejercicios: unos con pesas destinados a fortalecer el trapecio y los aductores del hombro; elongaciones y contracciones del dorso realizadas a expensas del trabajo de los pectorales, y elongaciones del cuello destinadas a relajar los escalenos.
Cada uno de los ejercicios, que se señalan a continuación debe ser repetido un mínimo 10 veces.
a. Encogimiento de los hombros: se realiza estando de pie, con ambos brazos en aducción sosteniendo pesas de 1 kg (peso que deberá incrementarse en forma progresiva en el curso del tratamiento). Deben llevarse ambos hombros simultáneamente hacia arriba y adelante hasta el máximo posible (Figura 15), volviendo luego a la posición de reposo; luego deberá repetirse el ejercicio, llevando ahora los hombros hacia arriba y atrás (Figura 16). Una vez que se toleran bien éstos movimiento podrá aumentarse el peso lentamente.
 Figura 15.
Figura 15. Figura 16.
Figura 16.b. Elevación de los hombros: partiendo desde la misma posición, manteniendo los codos rectos y con las pesas en las manos deben abrirse ambas extremidades superiores, elevando progresivamente los brazos hasta juntar ambas pesas por encima de la cabeza (Figura 17); luego se debe retornar lentamente a la posición de reposo. Una vez tolerado el ejercicio se deberá aumentar progresivamente el peso.
 Figura 17.
Figura 17.c. Elongación del dorso y de los pectorales: estando de pié contra la esquina de una pieza y con ambos pies separados deben levantarse los brazos hasta la altura de los hombros, apoyando las manos sobre las paredes contiguas mientras se mantienen los codos ligeramente flectados y el abdomen contraído; lentamente al tiempo que se inhala se debe cargar el cuerpo contra la esquina, flectando los codos hasta contactar con los muros, para luego retornar lentamente a la posición inicial, empujando con los brazos mientras se expira (Figura 18).
 Figura 18.
Figura 18.d. Extensión del dorso: se realiza en posición de decúbito ventral y con las manos entrelazadas en la parte baja de la espalda; se debe elevar la cabeza y el tórax tan alto como sea posible, empujando los hombros hacia atrás y con el mentón contraído, inhalando lentamente mientras se llega a la posición más elevada (Figura 19). Mantener ésta posición mientras se cuenta hasta tres para luego exhalar, retornando lentamente a la posición de reposo.
 Figura 19.
Figura 19.e. Movilización de la cintura escapular: se realiza en decúbito dorsal y con una pequeña almohada bajo los hombros. Mientras se inhala lentamente se elevan los brazos estirados, llevándolos hacia arriba y atrás por sobre la cabeza (Figura 20); luego se retorna a la posición inicial exhalando lentamente.
 Figura 20.
Figura 20.f. Movilización del cuello: se debe permanecer sentado y mirando hacia el frente, girando la cabeza primero hacia un lado hasta el máximo posible, para luego retornar a la posición de reposo; repetir la operación ahora hacia el otro lado; luego flectar el cuello (Figura 21), llevando el mentón hacia el tórax y volver a la posición previa; después extender el cuello hacia atrás, tanto como sea posible (Figura 22) y retornar a la posición de reposo; recostar entonces la cabeza sobre el hombro de un lado tanto como sea posible (Figura 23), para luego volver a la posición de reposo; repetir el ejercicio sobre el hombro contrario; finalmente flectar el cuerpo tanto como sea posible instalando la cabeza entre las rodillas; en esa posición girar lentamente el cuello en forma circular, manteniendo los músculos del cuello relajados (Figura 24).
 Figura 21.
Figura 21. Figura 22.
Figura 22. Figura 23.
Figura 23. Figura 24.
Figura 24.TRATAMIENTO QUIRÚRGICO
Deberá reservarse para los pacientes que previamente han presentado alguna complicación arterial o venosa; en forma ocasional para algunos casos con complicaciones neurológicas severas o ante el fracaso del tratamiento kinésico.
Se trata de una intervención quirúrgica dirigida a liberar el paquete neurovascular a través de la ampliación del espacio costoclavicular, mediante la remoción del agente compresivo que ha sido sospechado durante el estudio y comprobado en el curso de la intervención.
- Esta puede consistir en la resección extraperióstica de la primera costilla, aunque no en toda su longitud sino particularmente en su arco anterior, que es el que contiene el tubérculo del escaleno, intervención que debe realizarse cada vez que demuestre que ésta puede tener un rol compresivo, lo que necesariamente implica realizar una escalenotomía anterior o bien, como ocurre en la mayoría de los casos con sólo hipertrofia del escaleno, en la ejecución de una escalenotomía anterior, la que deberá siempre ir acompañada de la resección de por lo menos parte del arco anterior de la primera costilla para dificultar una eventual reinserción del escaleno (Figura 25).
 Figura 25. Esquema de la liberación neurovascular que se obtiene luego de resecar la primera costilla y el escaleno anterior.
Figura 25. Esquema de la liberación neurovascular que se obtiene luego de resecar la primera costilla y el escaleno anterior.- En algunas ocasiones puede ser necesario resecar una costilla cervical Figura 26), una apófisis transversa larga o seccionar además aquéllas bandas fibromusculares anómalas que se comprueben compresivas, o completar la liberación neurovascular seccionando a veces el escaleno medio, el subclavio e incluso parte del pectoral menor para lograr éste propósito.
 Figura 26. Esquema de la liberación neural después de realizada la resección de una costilla cervical.
Figura 26. Esquema de la liberación neural después de realizada la resección de una costilla cervical.- Cada vez que se advierta una deformación fibrosa del perineurio de las raíces del plexo braquial originada por la compresión mantenida, como suele ocurrir en los casos neurológicos más graves, resulta útil complementar la liberación agregando una neurolisis del plexo, la que se realiza abriendo ampliamente el perineurio en forma longitudinal con el objeto de eliminar ésta posible causa residual de compresión neurológica.
A. TÉCNICAS DESCOMPRESIVAS:
El síndrome puede ser corregido en forma adecuada utilizando diversas vías de abordaje, cada una de las cuáles tiene sus indicaciones, ventajas e inconvenientes.
ABORDAJE POR VÍA CERVICAL
La vía cervical puede ser utilizada para remover una costilla cervical, realizar escalenotomías o remover la primera costilla, pero su mejor indicación surge cada vez que, aparte de liberar el paquete neurovascular, se desee reparar en alguna forma los vasos subclavios.
Esta técnica propuesta inicialmente por Falconer y Lee, resulta útil para realizar una escalenotomía, pero inadecuada si se pretende remover la primera costilla; sin embargo con la modificación de Nelson (16) permite cumplir ambos objetivos.
Con el paciente en decúbito dorsal y los hombros elevados debe colocarse la extremidad superior en aducción y rotar la cabeza hacia el lado opuesto, realizando una incisión en la base del cuello de unos 8-10 cm y paralela a la clavícula, desde el esternocleidomastoídeo hacia afuera, seccionando o retrayendo el músculo omohioídeo para luego disecar la grasa pre escalénica; una vez disecado y protegido el frénico, se rodea el escaleno anterior con una pinza en ángulo recto y se secciona en su base (Figura 27).
 Figura 27. Abordaje del síndrome del opérculo torácico por vía cervical.
Figura 27. Abordaje del síndrome del opérculo torácico por vía cervical.Luego, si se desea resecar la primera costilla, deberá disecarse y rodear la arteria subclavia con una cintilla, procediendo a despegarla de la cúpula pleural y a seccionar aquéllas ramas que impiden movilizarla, con excepción de la vertebral (Figura 28).
 Figura 28. Despegamiento del periostio de la primera costilla.
Figura 28. Despegamiento del periostio de la primera costilla.Para resecar la primera costilla deberá movilizarse tanto la arteria subclavia como el plexo braquial que luego se traccionan mediante un separador de vena, tras lo cuál se procede a liberar las diversas conexiones fasciales de la primera costilla con la ayuda de un elevador perióstico, para luego resecarla en forma extensa incluyendo el periostio, y teniendo especial cuidado al resecar su porción anterior que es la más compresiva; se puede utilizar para ello una gubia de mordida lateral como son las de Raney o de Kerrison (Figura 29).
 Figura 29. Una buena forma de resecar la primera costilla a través de la vía cervical.
Figura 29. Una buena forma de resecar la primera costilla a través de la vía cervical.Una vez completada la maniobra, deberá comprobarse la eficacia de la liberación introduciendo un dedo en la zona al tiempo que se moviliza ampliamente la extremidad en todas direcciones (17). Finalmente se instala un drenaje aspirativo.
ABORDAJE POR VÍA AXILAR
Esta vía fue propuesta por Roos en 1967 (18, 19) y, pese a tratarse de una técnica difícil, ha llegado a constituir el acceso de elección para aquéllos pacientes en los cuales se requiere obtener la liberación del paquete neurovascular resecando la primera costilla o las bandas compresivas anómalas, ya que permite una excelente liberación de las estructuras comprometidas. No resulta útil en aquéllos casos en que debe además efectuarse alguna reparación vascular, ya que el campo que permite obtener es demasiado reducido como para permitir realizarlas en buena forma.
El paciente deberá disponerse en decúbito lateral, firmemente sujeto para impedir su caída hacia adelante o atrás durante la intervención, disponiendo la mesa de operaciones muy baja y con la extremidad afectada preparada y envuelta en paños, para su posterior tracción y movilización por el ayudante.
Se realiza una incisión de curvatura superior justo a nivel del vello axilar, extendida entre el pectoral mayor y el dorsal ancho, disecando directamente hacia el plano costal.
Cada vez que sea posible deberá evitarse seccionar el nervio intercostobraquial, para evitar una hipostesia prolongada del brazo, y el nervio torácico largo cuya lesión dejará una escápula alada, así como debe evitarse las elongaciones del plexo en forma prolongada o desmedida, a objeto de impedir neuropraxias de lenta recuperación.
Para tal efecto resulta imprescindible la colaboración del ayudante, quién deberá traccionar y levantar la extremidad cada vez que el cirujano trabaja en el área axilar, para lo cuál resulta extraordinariamente útil que realice la separación mediante su antebrazo, flectado, bajo el antebrazo flectado del paciente, debiendo aliviar la tracción en forma intermitente para permitir la recuperación vascular y neurológica del miembro (Figura 30).
 Figura 30. Posición del paciente y forma adecuada de exponer la zona operatoria mediante la tracción de la extremidad.
Figura 30. Posición del paciente y forma adecuada de exponer la zona operatoria mediante la tracción de la extremidad.Completada la disección roma preferentemente realizada con tórulas de disección, podrá identificarse claramente el trayecto vertical de la vena axilar y por detrás la inserción del escaleno anterior, que resulta conveniente seccionar en ese momento, luego de disecarlo y rodearlo con una pinza en ángulo recto (Figura 31); con la ayuda de una tijera curva larga y de las ruginas de Overholt debe disecarse completamente la porción anterior de la primera costilla, incluyendo su periostio, de todas las estructuras vecinas mientras la tracción del ayudante aleja los vasos y las ramas del plexo braquial (Figura 32), para luego proceder a su resección extraperióstica intentando impedir su regeneración (Figura 33).
 Figura 31. Esquema de la operación a través de la vía axilar. A) Línea de la incisión. B) Presentación de los diversos elementos del paquete neurovascular y de los musculoaponeuróticos.
Figura 31. Esquema de la operación a través de la vía axilar. A) Línea de la incisión. B) Presentación de los diversos elementos del paquete neurovascular y de los musculoaponeuróticos. Figura 32. Separación exponiendo la primera costilla en el fondo de la incisión, para su resección extraperióstica y posterior resección.
Figura 32. Separación exponiendo la primera costilla en el fondo de la incisión, para su resección extraperióstica y posterior resección. Figura 33. Esquema de la disposición de las diversas estructuras del opérculo torácico derecho una vez removida la primera costilla. 1) Extremo posterior de la resección costal. 2) Extremo anterior.
Figura 33. Esquema de la disposición de las diversas estructuras del opérculo torácico derecho una vez removida la primera costilla. 1) Extremo posterior de la resección costal. 2) Extremo anterior.Puede realizarse con facilidad la sección anterior y posterior de la costilla si se emplea un costótomo articulado curvo y angulado de primera costilla; en su defecto, se pueden realizar ambas secciones por parcialidades, mediante una gubia de mordida lateral de Kerrison o de Raney (Figura 34).
 Figura 34. Instrumental de elección para realizar la corrección del SOT a través de la vía axilar: ruginas de Overholt, costótomo de primera costilla y gubias de mordida recta y lateral.
Figura 34. Instrumental de elección para realizar la corrección del SOT a través de la vía axilar: ruginas de Overholt, costótomo de primera costilla y gubias de mordida recta y lateral.Cuando se prevé que la resección costal realizada en esa forma puede resultar riesgosa, es lícito realizar una sección costal en la mitad de la costilla que se intenta resecar, tras lo cuál podrán ser disecados y resecados con mayor seguridad ambos segmentos costales traccionados y elevados con la ayuda de una pinza de Kocher; en cada caso las porciones más lejanas de la costilla podrán ser resecadas por parcialidades mediante una gubia larga de curvatura lateral (Figura 35).
 Figura 35. Costótomo alternativo que permite eliminar la primera costilla por parcialidades.
Figura 35. Costótomo alternativo que permite eliminar la primera costilla por parcialidades.Luego deberá explorarse buscando bandas o inserciones musculares anómalas y proceder a su sección, para lo cuál resulta extremadamente útil la exploración digital mientras se moviliza la extremidad en diversas direcciones.
Si la pleura está indemne, lo que deberá comprobarse siempre con suero, basta con instalar un drenaje de Penrose y si fue abierta durante el procedimiento como ocurre casi en la mitad de los casos, deberá instalarse un drenaje intrapleural fino aspirativo bajo agua, tras lo cuál la herida se cierra en un plano, con sutura continua del celular y la fascia con ácido poliglicólico, y la piel con nylon.
Cada caso deberá controlarse con radiografía en las horas siguientes por la eventualidad de un neumotórax, que puede complicar la evolución habitualmente benigna si no es advertido y tratado.
ABORDAJE POR VÍA POSTERIOR
Fue propuesto por Clagett, quién realizaba un abordaje bastante similar al de una toracoplastia y modificado posteriormente por Martinez, quién la convierte en una intervención poco invasiva (20, 21) que, si bien deja una cicatriz extensa en el dorso y puede complicarse por atrofia de la musculatura interescapular, permite obtener la mejor exposición del área comprometida, acceder bien a la primera costilla, a una costilla cervical y a las bandas fibromusculares anómalas, haciendo difícil la lesión de vasos y plexo debido a la lejanía con que éstos se presentan. Resulta ideal para reoperar pacientes recidivados o que hayan sido antes operados en forma incompleta.
El paciente es enfrentado por atrás, dispuesto en decúbito lateral y con la extremidad afectada hacia arriba tras lo cuál se realiza una incisión curva siguiendo el borde interno de la escápula en toda su extensión (Figura 36).
 Figura 36 a y b: Abordaje posterior. a) Posición del paciente y ubicación de la incisión. b) Exposición de los planos musculares.
Figura 36 a y b: Abordaje posterior. a) Posición del paciente y ubicación de la incisión. b) Exposición de los planos musculares.
Luego y manteniendo intacto el dorsal ancho, deberá seccionarse el trapecio y el romboides a fin de permitir la rotación externa de la escápula, la que debe ser traccionada con un separador de Mayo que luego puede reemplazarse por un separador estático de Tuffier o de Finochietto; el nervio supraescapular debe ser respetado en ésta etapa a objeto de preservar la función posterior de la escápula.
Una vez identificada la primera costilla en la parte más alta de la incisión, podrá mejorarse su exposición si se realiza una corta resección subperióstica del extremo posterior de la segunda costilla, con la finalidad de obtener una depresión de la pared; luego se liberarán las estructuras musculares desde atrás hacia adelante, seccionando el escaleno posterior a nivel de su inserción en la segunda costilla, el escaleno medio cuando se inserta en el borde superior de la primera costilla y finalmente el escaleno anterior en su inserción (Figura 37).
 Figura 37 c y d: Abordaje posterior. c) Exposición de los planos musculares profundos. d) Aspecto del plano costal.
Figura 37 c y d: Abordaje posterior. c) Exposición de los planos musculares profundos. d) Aspecto del plano costal.
Todo el procedimiento que sigue puede realizarse con la ayuda de las ruginas de Overholt, hasta dejar la primera costilla liberada pero con su periostio intacto; luego, mediante un costótomo de primera costilla, se procede a seccionar la costilla en su parte anterior a nivel del cartílago y después en su extremo posterior, liberando las bandas anómalas que pudieran existir y las ramas del plexo braquial, tras lo cuál cabe instalar un drenaje cuando la pleura no ha sido abierta, o intrapleural y espirativo cuando ello ha ocurrido, y cerrar la incisión por planos.
Independientemente de la vía de abordaje empleada, los resultados de la descompresión neurovascular son extremadamente buenos si se realiza una cuidadosa selección de los pacientes y se aplica una técnica quirúrgica adecuada, resultando normal esperar que los síntomas neurológicos desaparezcan de inmediato después de la cirugía (Figura 38).
 Figura 38. Fotopletismografía dinámica en un paciente operado bilateral. Es posible advertir un aumento de la amplitud del registro, hecho característico cada vez que se ha obtenido una liberación neurovascular adecuada.
Figura 38. Fotopletismografía dinámica en un paciente operado bilateral. Es posible advertir un aumento de la amplitud del registro, hecho característico cada vez que se ha obtenido una liberación neurovascular adecuada.Como en las primeras 4-6 semanas no es raro encontrar cierto grado de espasmo muscular, dolor o hipostesias en la zona operatoria, borde posterior del brazo o región escapular debidos a la separación de los nervios y la elongación del plexo, es conveniente iniciar un tratamiento kinésico precoz y de corta duración para acelerar la recuperación motora de la extremidad y del cuello, ya que la recuperación sensitiva de eventuales déficit neurológicos quirúrgicos será más lenta.
Todas las recurrencias del síndrome, que han sido descritas en el 4-9 % de los pacientes requerirán una cuidadosa reevaluación diagnóstica, la que podrá demostrar si son debidas a la presencia de patología concomitante no corregida, como son los síndromes del túnel carpiano, a una descompresión incompleta o insuficiente, como ocurre cuando se extrae la segunda costilla en lugar de la primera, una primera costilla sin resecar las bandas fibrosas compresivas, o se extrae la costilla cervical pero no la primera costilla, o a una posible reinserción costal del escaleno, de frecuente ocurrencia cuando se secciona sin resecar la primera costilla, o por una reinserción de éste sobre la fascia de Sibson, la arteria subclavia o el perineurio.
B. TÉCNICAS VASCULARES REPARADORAS:
No están indicadas sino en aquéllos pocos casos en que se demuestre la presencia de una alteración vascular definitiva, originada por una compresión severa y prolongada, y cuya presencia signifique algún riesgo posterior para el paciente. Pueden realizarse de inmediato después de la descompresión neurovascular, o ser ejecutadas en forma diferida. Si bien muchas veces se trata de procedimientos quirúrgicos relativamente nuevos, en pleno desarrollo y evaluación, se pretende corregir con ellos el componente arterial o venoso que resultó lesionado en forma severa durante el tiempo que permaneció actuando el agente compresivo una vez que éste ha sido removido.
REPARACIONES ARTERIALES
Entre las intervenciones arteriales, cabe considerar la posibilidad de remover algunas áreas de la subclavia retraídas o estenosadas, alteraciones que se suelen corregir mediante endarterectomías localizadas, o una angioplastía seguida de parche venoso o protésico. Asimismo, incluye la eventual remoción de aneurismas subclavios secundarios a la compresión y originados a partir de la dilatación post estenótica del vaso, procedimiento que debe ser seguida de un reemplazo arterial por prótesis.
La metódica no difiere en sus aspectos técnicos de la forma como el mismo procedimiento es realizado a nivel de otras arterias, pero cuando se contemple la posibilidad de realizarlo en forma simultánea con una descompresión costoclavicular deberá preferirse la vía cervical o la posterior y en ningún caso la axilar, que dificulta enormemente una buena exposición de la arteria.
REPARACIONES VENOSAS
Aparte del tratamiento anticoagulante y la terapia fibrinolítica, especialmente indicados para tratar las trombosis venosas agudas relativamente recientes de la extremidad superior intentando prevenir una embolización pulmonar, y reducir las posibilidades de síndrome post trombótico, y que también pueden emplearse además de los antiplaquetarios siguiendo una descompresión con carácter de urgencia, son alternativas quirúrgicas válidas para casos seleccionados:
- La trombectomía venosa: se ha intentado la remoción del coágulo en casos de trombosis severas agudas para abreviar su evolución y en teoría para disminuir las secuelas. Se realiza empleando sondas de Fogarty, que se pueden introducir a través de una vena periférica o directamente en la subclavia cuando se la aborda por vía cervical, axilar o posterior. Los resultados de éste procedimiento aún poco difundido, parecen alentadores (22, 23).
- La endovenectomía de la subclavia o de la axilar: pese a ser ejecutada infrecuentemente, permite resecar el segmento estenosado de la vena desde su interior; después de abrir la vena ampliamente en sentido longitudinal por su cara anterior y luego de completada la resección, debe realizarse la fleborrafia en forma continua o, para evitar una estenosis, mediante la instalación de un parche venoso suturado a los bordes de la flebotomía (24, 25).
Con ésta técnica se han descrito buenos resultados iniciales en un porcentaje cercano al 90 % de los casos en que ha sido empleada, encontrándose pendiente la evaluación alejada del procedimiento.
- Injertos venosos: se han propuesto para aquéllos casos de oclusión limitada a una porción de la vena subclavia o de la axilar, como una alternativa a la endovenectomía destinada a obtener la derivación de la sangre venosa de la extremidad hacia el tronco venoso braquiocefálico, saltándose el área ocluida.
Estos injertos venosos pueden realizarse en dos formas diferentes:
- Mediante la instalación de un puente confeccionado con safena libre o con vena safena espiralizada que se implanta en forma término lateral tanto sobre la vena subclavia distal (o la axilar) como sobre la vena yugular del mismo lado, en la misma forma y mediante una técnica similar a como se realiza un by pass arterial carótido-subclavio.
- Es posible obtener también una derivación venosa funcionante mediante una movilización de la vena yugular, la que previamente debe ser ligada y desconectada en su parte más alta y luego descendida hasta llevarla a la vena subclavia o axilar, a la cuál se anastomosa (26, 27, 28).
Estas técnicas pioneras han sido capaces de mostrar hasta ahora un 67 % de buenos resultados inmediatos, en especial cuando en forma transitoria se les agrega una fístula A/V destinada a mejorar el inicialmente flujo a nivel de la derivación (29).
BIBLIOGRAFÍA
1. Peet, R., Henricksen, J., Anderson, T., et als. Thoracic outlet syndrome. Mayo Clin. Proc. 1956; 31: 281-5.
2. Crawford, F. Thoracic outlet syndrome. Surg. Clin. of NA 1980; 60(4): 947-56.
3. Fujitani, R., Mills, J. Isquemia aguda y crónica de las extremidades superiores I. Oclusión de vasos de gran calibre. Ann. Vasc. Surg. 1993; 7: 106-12.
4. Glass, B. The relationship of axillary vein thrombosis to the thoracic outlet compression syndrome. Ann. Thorac. Surg. 1975; 19: 613-6.
5. Jamieson, J. Venous complications of the thoracic outlet syndrome. Eur. J. Vasc. Surg. 1987; 1: 1-36.
6. Roos, D. Congenital anomalies associated with thoracic outlet syndrome. Am. J. Surg. 1976; 132: 771-8.
7. Devin, R., Branchereau, A., Pellisier, J., et als. Syndrome de compression du défilé costo-claviculaire par tumeur de la premiére côte. Chirurgie 1981; 107: 749-54
8. Barker, W. Revisión histórica del síndrome de compresión del desfiladero torácico. Anales Cir. Vasc. 1989; 3(4): 289-94.
9. Mercier, C., Houel, F., Tournigand, P. Les complications vasculaires des syndromes de la traversée thoraco-brachiale. Chirurgie 1981; 107: 433-8.
10. Salo, J., Varstela, E., Ala-Kulju, K., et als. Management of vascular complications in thoracic outlet syndrome. Acta Chir. Scand. 1988; 154: 349-52.
11. Sanders, R., Craigh, H. Obstrucción de la vena subclavia y síndrome del opérculo torácico: revisión de la etiología y del tratamiento. Anales Cir. Vasc. 1990; 4(4): 397-410.
12. Entin, M. Carpal tunnel syndrome and his variants. Surg. Clin. of NA 1968; 48(5): 1097-112.
13. Hempel, G., Rusher, A., Wheeler, C., et als. Supraclavicular resection of the first rib for thoracic outlet syndrome. Am. J. Surg. 1981; 141: 213-5.
14. Cuetter, A., Bartoszek, D. The thoracic outlet syndrome: controversies, overdiagnosis, overtreatment and recommendations for management. Muscle & nerve 1989; 12: 410-19.
15. Redford, J. Physical treatment, en Pollak, E.; Thoracic outlet syndrome: diagnosis and tratment, Mount Kisko, New York: Futura Publishing Company, Inc., 1986: 151-68.
16. Nelson, R., Dava, R. Thoracic outlet compression syndrome. Ann. Thor. Surg. 1969; 8: 437-42.
17. Thomas, G., Jones, T., Stavney, S., et als. Thoracic outlet syndrome. The Am. Surg. 1978: 2; 483-95.
18. Roos, D. Transaxillary approach for first rib resection to relieve thoracic outlet syndrome. Ann. Surg. 1966; 163: 354-9.
19. Gruss, J., Bartels, D., Tsafandakis, S., et als. Aspects chirurgicaux et résultats du traitement dans le thoracic-outlet-syndrom. Chirurgie 1980; 106: 406-8.
20. Clagett, O. Research and prosearch. J. Thorac. Cardiovasc. Surg. 1962; 44: 153-6.
21. Martinez, N. Posterior first rib resection for total thoracic outlet syndrome descompression. Cont. Surg. 1979; 15: 13-21.
22. De Weese, J., Adams, J., Gaiser, D. Subclavian venous thrombectomy. Circulation 1970; 41-42 (Suppl. II): 158-64.
23. Drapanas, T., Curran, W. Thrombectomy in the treatment of "effort" thrombosis of the axillary and subclavian veins. J. Trauma 1966; 6:107-19.
24. Campbell, C., Chandler, J., Tegtmeyer, C., et als. Axillary, subclavian and brachiocephalic vein obstruction. Surgery 1977; 82: 816-26.
25. Aziz, S., Straehley, C., Wheelan, T. Effort-related axillosubclavian vein thrombosis: a new theory of pathogenesis and a plea for direct surgical intervention. Am. J. Surg. 1986; 152: 57-61.
26. Doty, B., Baker, W. Bypass of superior vena cava with spiral vein graft. Ann. Thorac. Surg. 1976; 22: 490-3.
27. Jain, K., Smejkal, R. Use of spiral vein graft to bypass occluded subclavian vein. J. Cardiovasc. Surg. 1988; 29: 572-3.
28. Hasmonai, M., Schramek, A., Farbstein, J. Cephalic vein cross-over bypass for subclavian vein thrombosis: a case report. Surgery 1976; 80: 563-4.
29. Sanders, R., Rosales, C., Pearce, W. Creation and closure of temporary arteriovenous fistulas for venous reconstruction or thrombectomy: description of technique. J. Vasc. Surg. 1987; 6: 504-5.
29 comentarios:
BUENISIMO EL ARTICULO....muy completo....queda todo muy claro.Buenas imagenes de evaluaciòn.
Excelente.
Doctor, despues de algunos años de ser operado de SOT bilateral por Usted, me queda todo muy claro, se agradece la clara explicacion para mi y para todos
Ignacio Rojas
Dr. excelente articulo muy bien explicado,...me acaban de diagnosticar este Sindrome despues de 25 años de dolores y me estoy informando al respecto y quisiera saber si me puede responder lo siguiente: si con tratamiento kinesico mejorare, aunque el examen(pletismiografia bilateral) dice oclusion del flujo sanguineo extremidad derecha y disminucion severa del flujo sanguineo extremidad izquierda.
Mil gracias
Daniela Barra F.
Santiago
Doctor, me acaban de diagnosticar Sindrome de Operculo toracico derecho, como puedo ubicarlo, en que lugares atiende?.
Agradezco su ayuda,
Carolina Orellana.
agradezco la informacion, hacen dos años que fui diagnosticada, tengo costilla cervical bilateral y no a sido nada facil para mi, estoy pronta a la operacion, tengo temor de no quedar al 100% ya que estoy muy lastimada al esperar tantos años en saber que me sucedia. pero con el art. veo que no es demasiado complejo
Carolina Orellana:
Actualmente atiendo en forma privada en Providencia, Santiago y en Integramendica. Si haces llegar algun correo con todo agrado te enviaré mayores datos
Dr.
Exelente articulo, me aclara todas las dudas con relación a esta enfermedad que me acaban de diagnosticar,tengo una compresión dinámica moderada sobre ambas subclávias a nivel del opérculo,además de padecer fibromialgia, soy paciente de la Dra. Stevenson del hospital FACH, quién me derivó a kine... pero con cada sesión termino mas adolorida, sesiones que suspendí por el momento, ¿ es posible que pueda realizar los ejercicios que propone por mi cuenta mientras espero consulta ? Tengo 51 años y no tengo nada de fuerza en mis brazos.
MUCHISIMAS GRACIAS
SYLVIA F.v B.
Sylvia F:
Claro que puede realizar los ejercicos por su cuenta, le ayudarán de todas maneras.
Es raro que el tratamiento kinesico no la haya aliviado mas en forma rápida, pero pudiera ocurrir que la compresion dinámica arterial sea moderada en su caso pero la neural, responsable de la falta de fuerzas o el dolor que incluso puede simular una fibromialgia, sea extremadamente grave. Suerte.
Dr. R. Poblete
Muchas gracias por tan completa explicación.
Pero me gustaría saber que ocurre cuando no se le hace el tratamiento indicado y como abordar a un médico que quiere hacer caso omiso al diagnóstico.
Gracias
Jali:
Interesante comentario. Cuando un SOT plenamente demostrado no se trata en ninguna forma sigue a lo largo del tiempo un curso tórpido y claramente fluctuante pero con tendencia a empeorar lentamente. Puede aparecer alguna complicación arterial o venosa pero predominan las denervaciones que pueden ser muy invalidantes.
Existen colegas, particularmente neurólogos refractarios a cualquier cirugía, que rechazan ésta condición sin haber visto jamás uno de éstos pacientes, e ignorando las evidencias difíciles de refutar que ofrecen los métodos de estudio vasculares modernos. Por desgracia con su actitud claramente retrógrada continúan dejando al márgen del beneficio de un tratamiento adecuado a ciertos pacientes.
Frente a ésta situación, que en verdad todavía existe, sólo parece aconsejable recomendarle un cambio de especialista.
Dr. R Poblete
mi hijo tiene 7 años y padece el sindrome de operculo toracico he consultado algunos doctores dicen que no hay mas remedio que la cirugia lo que quiero saber si a esta edad que tan riesgoso es una operacion de este tipo, gracias espero su respuesta
emirjoshua_flf:
SOT que sean verdaderamente graves a esa edad son poco frecuentes, y algo mas difíciles de operar por el escaso tamaño de los elementos que deben ser tratadas en cada caso en particular, lo que obliga a extremar los cuidados para evitar complicaciones quirúrgicas. Minimizado el riesgo, y una vez obtenida una buena descompresión costo - clavicular la evolución post operatoria es, por lo menos en mi experiencia increíblemente buena, y mejor y más rápida que en los adultos.
Dr R Poblete
gracias por contestarme,doctor lo que se me paso comentarle es que mi hijo desde los 4 años sufre de dolor, entumecimiento, calambres e inflamacion en su brazo derecho aunque se ha agudizado el dolor estos ultimos meses y ha sido un va y ven.
de antemano le agradezco su atencion a mis dudas.
doctor, nuevamente sobre el asunto del niño de siete años, en el comentario anterior se me paso decirle que si con estos sintomas acelera mas su operacion. Gracias.
Realmente una información, muy buena,muy completa y lo mejor!! de fácil entendimiento para la mayoría de la población.
Muchas Gracias
DOCTOR MI SEÑORA TIENE ESCLEROSIS MULTIPLE BROTE /REMICION Y QUISIERA SABER SI PODEMOS TENER UNA CONSULTA CON USTED PARA SABER SI OPERANDOLA DEJA DE TENER BROTES.MUCHAS GRACIAS
Mi nombre es Leonardo me operaron en el septiembre de 2009, accedieron a la primera costilla por la axila.
Se me habia producido una trombosis venosa de la vena subclavia. La operacion salio bien, posteriormente me hicieron 1 angioplastia para desobstruccion de la vena en abril deL 2010 y a en agosto la tubieron que repetir porq se volvio a estrangular la vena en la misma zona, repetí el estudio con contranste y volvio nuevamente aparecer la compresion sobretodo con la maniobra del brazo derecho.
Me extrajeron la 1° costilla, me hicieron 2 angiplastias y los sintomas continuan. NO SE POR DONDE SEGUIR (TENGO FUERTES DOLORES CERVICALES, CUELLO Y EN LA ZONA DEL OMOPALATO. NO SE QUE MAS HACER DADO QUE ESTE NO ES MUY COMUN, POCOS MEDICOS CONOCEN ESTA PATOLOGIA
(permanecí anticugualado con simtron desde que epese con los sintomas de adormecimiento de miembro sup derecho)
ESCUCHO SUGERENCIAS, MUCHAS GRACIAS
Mi nombre es Leonardo me operaron en el septiembre de 2009, accedieron a la primera costilla por la axila.
Se me habia producido una trombosis venosa de la vena subclavia. La operacion salio bien, posteriormente me hicieron 1 angioplastia para desobstruccion de la vena en abril deL 2010 y a en agosto la tubieron que repetir porq se volvio a estrangular la vena en la misma zona, repetí el estudio con contranste y volvio nuevamente aparecer la compresion sobretodo con la maniobra del brazo derecho.
Me extrajeron la 1° costilla, me hicieron 2 angiplastias y los sintomas continuan. NO SE POR DONDE SEGUIR (TENGO FUERTES DOLORES CERVICALES, CUELLO Y EN LA ZONA DEL OMOPALATO. NO SE QUE MAS HACER DADO QUE ESTE NO ES MUY COMUN, POCOS MEDICOS CONOCEN ESTA PATOLOGIA
(permanecí anticugualado con simtron desde que epese con los sintomas de adormecimiento de miembro sup derecho)
ESCUCHO SUGERENCIAS, MUCHAS GRACIAS
Leonardo:
La trombosis venosa del miembro superior es una posible complicación venosa del SOT.
Cuando se tratan con anticoagulantes, angioplastias o cirugía los síntomas desaparecen lentamente con el tiempo y lo único que puede persistir es cierto grado de edema del brazo.
Si como parece tienes aún molestias neurológicas habría que revisar si realmente desapareció completamente la compresión neural, que es lo que pretende la cirugía, si existe una lesión neural definitiva y si se resecó realmente el arco anterior de la primera costilla. Con la experiencia que tengo una vez resequé por error el arco anterior de la segunda y he tenido que reoperar algunos casos por el mismo motivo.
Necesitas que te hagan un buen estudio de parrilla costal, un estudio electrofisiológico y un estudio arterial pero en reposo y además dinámico pero con pletismografía y fotopletismografía y no un imple eco doppler para descartar estas posibilidades
Suerte
Guillermo Otoya
Estimado Dr. tengo un paciente con quilotorax izquierdo, probablemente secundario a trombosis de subclavia secundaria a via central. dificil de demostrar pero es el unico antecedente. Esta con NPT sin mejoria. Propone alternativa quirurgica? Muchas gracias¡¡
HOLA DOCTOR MUY INTERESANTE SU ARTICULO, UNA PREGUNTA TENDRA USTED ALGUNA INFORMACION DE LA UTILIDAD DEL DOPPLER EN ESTE SX DE OPERCULO O EN SU EXPERIENCIA NO LE SERIA UTIL, GRACIAS, DESDE MEXICO D.F.
Hola doctor yo quisiera saber un poquito mas resumido pq tengo mi prima cn ese problema y quisiera saber mucho mas y cmo son los pasos a seguir gracias soy Carla Yaguno d San Pedro Buenos Aires...Mi correo es lagatyta-18@hotmail.com
Me acaban de diagnosticar esto, llevo como 4 años con los dolores pero yo pensaba que era estrés! Después de haberme percatado de que tenía morada la mano me mandaron a un Angiólogo, mismo que me mando a un estudio de doppler en el brazo afectado, es así como detectaron el síndrome.
Mi tratamiento será de ejercicios por 3 meses y si no hay mejora tendrán que operarme.
Mis síntomas ya son patéticos, todo el día traigo dormida, hormigueando el brazo, dolores espantosos, se me pinta la mano mas obscura, me refiero a que creo que ya deje avanzar mucho la enfermedad como para que me cure con la rehabilitación física y por una falta de diagnóstico oportuno pues creo que tendrán que operarme.
Quiero felicitar al autor del artículo... más claro ni el agua.
HOLA SOY GISELA YEPEZ 48 AÑOS DE VENEZUELA ME OPERARON DE OPERCULO SUPERIOR DERECHO EN MARZO 2014 LLEVO 3 MESES DE TERAPIAS, PERO IGUAL ESTO ME PRODUCE MUCHO DOLOR EN AMBOS BRAZOS Y MANOS QUIERO SABER SI ESTO DEBE DESAPARECER, YA QUE DURE 8 HORAS EN PABELLON Y PARA MI Y MI FAMILIA ES VERDADERAMENTE TRAUMATICO DR. DE VERDAD QUE PUEDO HACER
ESTARE PENDIENTE DE SU RESPUESTA YA QUE MI MEDICO ES EXCELENTE
Dr Ricardo Balcázar: Gracias por su preocupación por el diagnóstico del SOT. Nuestra experiencia nos ha convencido que el eco doppler solo resulta de utilidad para estudiar únicamente los SOT predominantemente arteriales y sobre todo cuando son graves, ya que en ellos demuestra un cese del flujo hacia el brazo durante las maniobras posicionales o durante el reposo. En la inmensa mayoria de los SOT que son predominantemente neurales y venosos el eco doppler resulta de muy poca utilida dpara confirmarlos. En éstos son ideales los estudios arteriales de los miembros superiores con doppler mas pletismografía, en reposo y dinamicos que no solo loc confirman sinompermiten evaluar su severidad en globo
Atte
Dr Raúl Poblete
Gisela:
Para opinar con mayor fundamento y poder estimar como seguirá tu futuro es indispensable poder disponer de algunos antecedentes complementarios acerca de tu enfermedad. Interesaría saber los síntomas previos y su data, los métodos de estudio que se utilizaron en especial la radiografia de tórax para poder ver las primeras costillas y algún estudio vascular realizado antes de la cirugía, el tipo de cirugia realizada y mediante que via, el tipo de trat kinesico que estás realizando y si estás tomando algún medicamento a la fecha.
Contestame a mi correo raulps@vtr.net y con todo gusto intentaré apoyarte en relación con tu problemática actual
Atte
Dr Raúl Poblete
saludos dr fui operado de la cosilla cervical me la quiataron por el cuello hace ya 1 ano y medio por que me obstrullo la arteria subclavia y el brazo se me lleno de cuagulos me pusieron un bay pass hoy en dia tengo calambres en los dedos y en el area del cuello donde me abrieron eso ahi me hala y nunca me di terapia que debo hacer este malestar me tiene desesperado mi operacion fue en el lado derecho gracias
Publicar un comentario